▎藥明康德内容團隊編輯
2022年2月8日,優瑞科生物(Eureka Therapeutics)宣布,美國FDA已授予在研T細胞療法ET140203和ECT204治療肝細胞癌(HCC)的孤兒藥資格。這兩款T細胞候選産品均基于其專有ARTEMIS技術平台開發,靶向特異性肝癌抗原。優瑞科生物目前正在3項1/2期臨床試驗中招募患者,以分别評估它們的安全性和潛在療效。
肝癌是全球癌症相關死亡的主要原因之一。據估計,2020年全球肝癌新發病例超過90.5萬,死于該病的人數超過83萬。HCC是最常見的一種肝癌,約占75%~90%的原發性肝癌病例。在世界範圍内,增加HCC風險的主要因素是慢性乙型肝炎和慢性丙型肝炎、飲酒和代謝綜合征。
ARTEMIS平台有兩個核心功能組分:基于抗體的抗原結合結構域和效應結構域。ARTEMIS的受體設計讓它能夠利用内源性T細胞受體(TCR)通常采用的活化和調節途徑。因為這種政策沒有直接将細胞内信号域與共刺激域相連,有望消除T細胞過度活化引起的細胞因子釋放綜合征(CRS)。
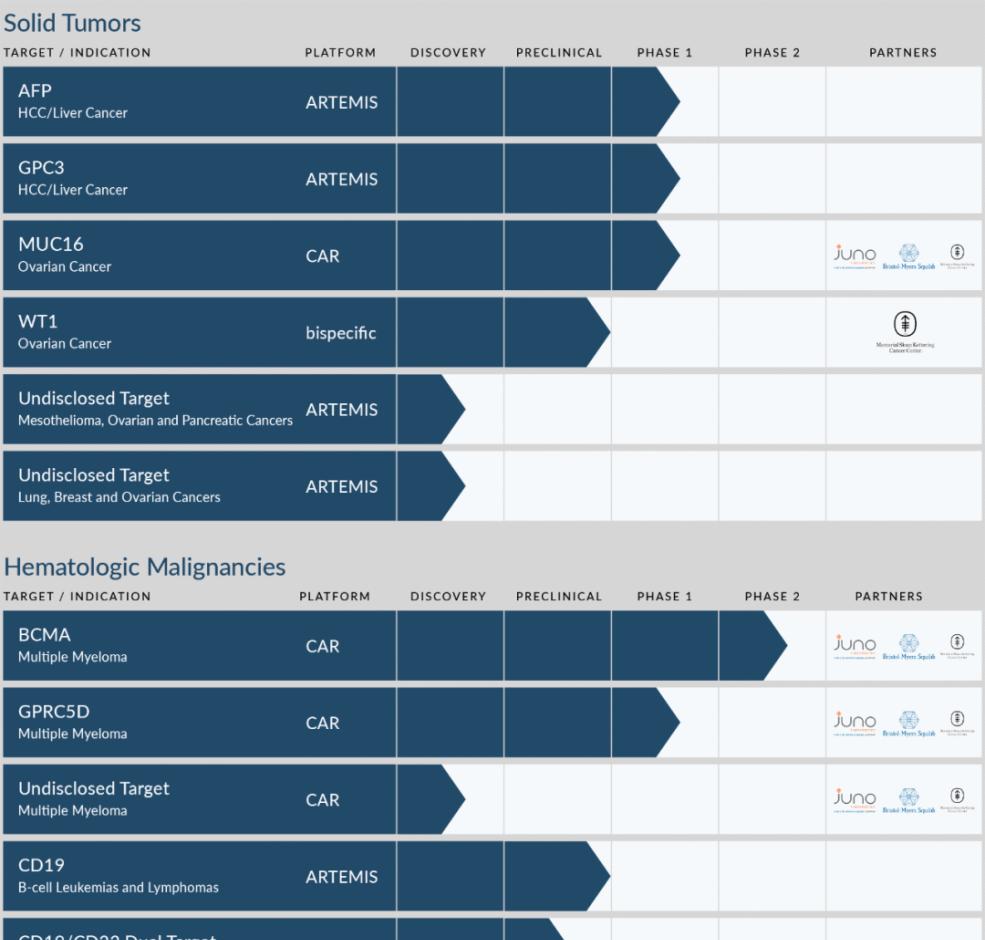
▲優瑞科生物産品管線(圖檔來源:優瑞科生物公司官網)
ET140203的治療過程通過采集患者的T細胞,對其進行工程化處理以表達優瑞科生物專有的ARTEMIS細胞受體,并回輸至患者體内。經修飾的ET140203 T細胞表達的受體靶向肝癌細胞上表達的甲胎蛋白(AFP)-肽/HLA-A2複合物。此外,ET140203 T細胞還整合了優瑞科生物專有的惡性良性腫瘤浸潤技術,動物模型已證明這能提高藥物浸潤實體瘤的能力,有望提高患者療效。該療法目前正在兩項開放标簽、劑量遞增、多中心的1/2期臨床試驗中進行評估,一項在AFP陽性的HCC成人患者中開展,一項在AFP陽性且患有複發性/難治性肝母細胞瘤(HB)、未另行指定的肝細胞惡性良性腫瘤(HCN-NOS)和HCC的兒科受試者中開展。
ECT204靶向肝癌細胞上表達的GPC3,GPC3是一種有前景的HCC抗原,存在于超過70%的HCC細胞。ECT204 T細胞也整合了優瑞科生物專有的惡性良性腫瘤浸潤技術。目前正在一項1/2期臨床試驗中接受評估,用于治療GPC3陽性的HCC成人患者。
▲優瑞科生物首席執行官劉誠博士