▎药明康德内容团队编辑
日前,Applied Molecular Transport(AMT)公司宣布,其口服IL-10细胞因子在研疗法AMT-101,单药治疗慢性结肠袋炎(一种难治性炎症性肠病)患者的2期临床试验取得了积极的顶线结果。独立数据监查委员会(DMC)基于对安全性和疗效数据的审评,建议将AMT-101推进至3期临床研究,以3 mg剂量治疗慢性结肠袋炎。
接近30%的溃疡性结肠炎(UC)患者最终需要完全切除结肠。接受名为回肠肛管吻合术(IPAA)可让切除结肠和直肠后患者仍能正常排除废物。然后手术后留些的袋壁可能出现炎症,称为结肠袋炎(pouchitis)。结肠袋炎临床表现为排便次数过多、尿急、粪便失禁、夜间渗液及下腹部疼痛等。目前美国尚无获批治疗方法。急性结肠袋炎通常对抗生素治疗有应答,但高达50%的结肠袋炎患者发展为慢性结肠袋炎,患者疾病经常复发或对抗生素治疗无应答。
AMT-101是一种新型的胃肠道选择性、口服IL-10疗法。AMT公司对霍乱弧菌分泌的Cholix蛋白进行改造,让它成为协助生物制品穿越肠上皮障碍的载体。Cholix蛋白通过与肠上皮表面的受体结合,能够利用胞吞作用穿过上皮细胞进入血液循环。AMT-101将基于Cholix蛋白开发的载体与IL-10构成融合蛋白,辅助IL-10穿过肠道上皮,并且聚集在肠道炎症的发生部位,潜在避免全身给药可能带来的副作用。它目前正在4项2期临床试验中用于治疗慢性结肠袋炎、溃疡性结肠炎和类风湿关节炎(RA)。
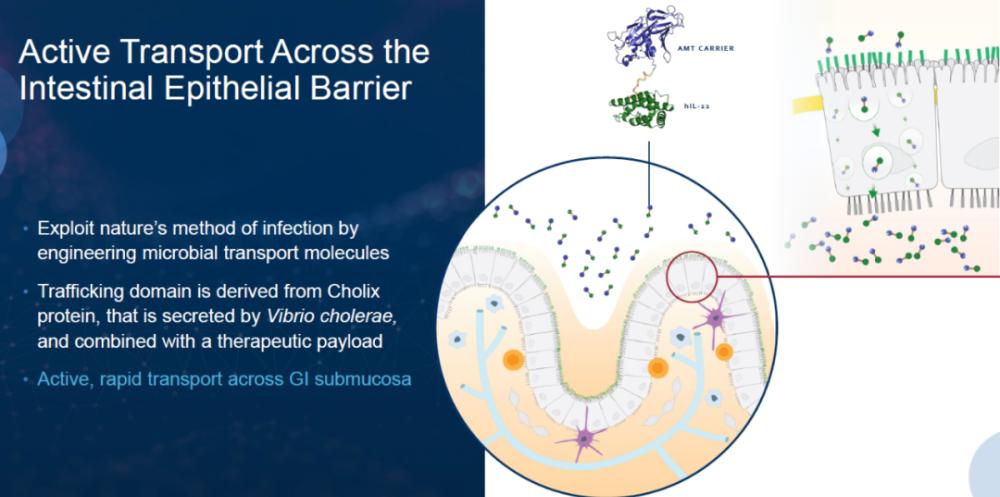
▲AMT公司的载体技术(图片来源:AMT公司官网)
这项双盲2期临床试验纳入22例慢性结肠袋炎患者,随机分配至接受3 mg或10 mg口服AMT-101的治疗。试验结果显示:
结合两个剂量组的患者数据,36.4%(8/22)的患者的排便频率获得改善。早在第2周,两个剂量组中就已观察到排便频率应答,并在整个治疗期间持续存在。顶线中期数据显示排便紧迫感、尿失禁和腹部绞痛等其他症状改善。两个剂量组中达到症状性排便频率改善的患者比例均超过了推进项目进入3期临床试验的标准。
组织学检测方面,22.7%(5/22)的患者达到了预先设定的Geboes评分≤3.1的组织学愈合应答,这是疾病改善的客观评估。患者的中位基线Geboes评分为5.1,表示重度结肠袋炎伴溃疡和组织破坏。两个剂量组均显示出组织学愈合应答。
▲AMT-101的关键疗效终点结果(图片来源:参考资料[1])
AMT-101观察到的安全性和耐受性良好。不良事件大多为轻度至中度,仅观察到1起严重不良事件,为巨细胞病毒(CMV)感染,这被确定与研究药物无关。
“我们很兴奋能与美国FDA和其他监管机构分享这些数据,以推进AMT-101在慢性结肠袋炎中的开发。”AMT首席医学官Bittoo Kanwar医学博士说,“我们相信这些数据支持AMT-101在治疗粘膜免疫学和炎症相关疾病方面的潜力。”
参考资料:
[1] Applied Molecular Transport Announces Positive Top-line Phase 2 Results from FILLMORE Trial of Oral AMT-101 in Patients with Chronic Pouchitis. Retrieved April 25, 2022, from https://ir.appliedmt.com/news-releases/news-release-details/applied-molecular-transport-announces-positive-top-line-phase-2
免责声明:药明康德内容团队专注介绍全球生物医药健康研究进展。本文仅作信息交流之目的,文中观点不代表药明康德立场,亦不代表药明康德支持或反对文中观点。本文也不是治疗方案推荐。如需获得治疗方案指导,请前往正规医院就诊。
版权说明:本文来自药明康德内容团队,欢迎个人转发至朋友圈,谢绝媒体或机构未经授权以任何形式转载至其他平台。转载授权请在「药明康德」微信公众号回复“转载”,获取转载须知。
分享,点赞,在看,聚焦全球生物医药健康创新