首例豬心髒移植到人體的手術成功,讓苦等器官移植的患者看到希望。異體器官移植為何鐘愛“豬萬能”?倫理問題如何解決?
曆經 7 小時的手術,一顆經過基因編輯的豬心髒在 57 歲的大衛·貝内特(David Bennett)的體内重新跳動起來。這也是全球首例豬心髒移植到人體的手術。
“這是一次豪賭”。大衛曾接受過豬瓣膜移植,此次心髒病情再次惡化,會診确定不适合接受傳統心髒移植手術後,豬心髒移植成為他活下去的最後選擇。經過美國監管機構緊急授權以及病患同意後,馬裡蘭大學醫學中心為他實施了這項手術。術後最關鍵的 48 小時裡,患者沒有發生任何異常,但仍連接配接着各種醫療儀器,醫生們也在密切監測着随時可能發生的感染、器官排斥等風險。
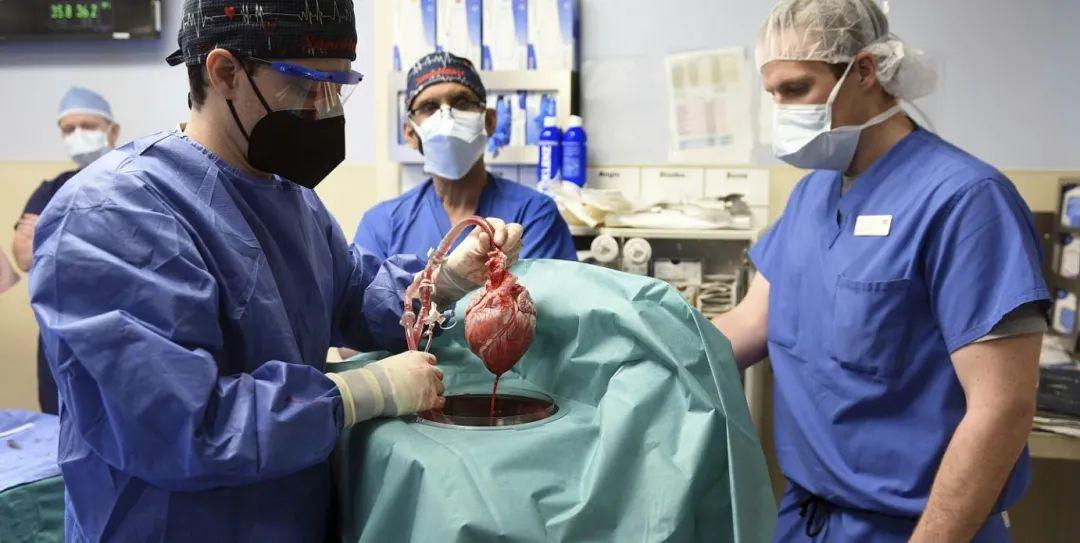
▲2022年1月7日,美國馬裡蘭州的醫生首次将基因編輯豬的心髒移植到了人類患者大衛·貝内特身上(圖檔來源:視覺中國)
盡管如此,在人類器官供應緊張的現實面前,這次手術仍給異種器官移植帶來了新的想象空間。
異種器官移植能否複興
器官移植主要有兩個分支,一種是“同種異體器官移植”,也就是接受器官移植的受體和供體是同一種類,比如人與人之間的器官移植;還有一種是“異種器官移植”,比如将動物的器官移植到人體中。
目前,在臨床上進行的器官移植手術,絕大多數是同種異體器官移植,但由于供體數量不足,很多人到生命的最後一刻也無法等到适合的器官。
據專家估算,大陸每年需要進行器官移植來挽救生命的患者大約有 30 萬。2020 年,大陸器官供體與受體的比例為 1∶15。每15 個等待的患者有一個可以獲得救命的器官,狀況雖有緩解,但仍有大量患者在等待中離去。
為緩解器官移植嚴重“供不應求”的沖突,科學家們很早開始嘗試動物器官替代的方法,開展異種器官移植也成為世界公認解決器官短缺的重要途徑。
哪些動物能夠擔當器官移植的供體呢?人們最先想到的是與人類親緣關系密切的猴、猩猩和狒狒。它們與人類同屬于靈長類,器官結構、生理功能、新陳代謝與人類相似。
▲X 光機下人、猴、豬的圖解(圖檔來源:視覺中國)
早在 20 世紀 60 年代,外科醫生曾試圖将猩猩的器官移植到人類身上。受體免疫系統很快對移植的器官産生了排斥,導緻移植器官在短時間内發生功能衰竭,進而導緻接受器官移植者的死亡。初期探索的反複失敗,讓人們意識到,靈長類的“近親”們可能并不是理想的器官移植供體。
而将靈長類列為器官供體候選者也面臨着包括技術、倫理在内的諸多問題。靈長類中大多數體型較小的種類,其器官性能和尺寸又無法承擔人類代謝的需要;靈長類繁殖率較低,且體型較大的猩猩和狒狒,本身處于瀕危狀态,也難以滿足人類對器官移植數量的需求。與人類是“近親”的它們,還可能帶有一些人類易感染的病毒,如猴免疫缺陷病毒和埃博拉病毒等,一旦這些器官移植到人體上,發生重組後可能産生更有害的病毒。種種的不利因素,使得靈長類候選者們的“光環”暗淡下來。
科學家們又将目光轉到了體型、食性、代謝水準等外在名額與人類接近的動物身上。經過層層“篩選”,因器官大小與人類相仿,傳染病風險較低,數量相對更為充足等優勢,豬被認為是現階段異種器官移植的最佳選擇對象。
從性能參數來看,豬與人的體溫均為 36℃~ 37℃,心髒大小、管道分布和動力輸出,甚至心率(人的心率為 60 ~ 100 次 / 分鐘,豬為55~60次/分鐘)都相類似。可預見的器官移植範圍包括角膜、皮膚、胰島、關節、肌腱、韌帶、腎髒、心髒、肝髒等多方面。
在醫學界,植入人體細胞的豬的心髒瓣膜已經用于患者治療,豬的韌帶肌腱移植也已經成熟。
2017 年 9 月,在美國巴爾的摩召開的第 14 屆國際異種移植協會大會上,亞特蘭大埃默裡大學團隊宣布他們實驗室的一隻猕猴接受了基因改造過的豬腎髒的移植後400多天才發生排斥反應,比此前記錄延長了數個月。德國慕尼黑大學團隊在狒狒身上進行了豬心髒移植,移植物堅持了 90 天。
▲德國的研究人員給多隻狒狒從豬身上移植心髒,狒狒存活了90 天(圖檔來源:Nature)
同時,小部分生物工程公司利用基因編輯技術,通過敲除部分豬的基因和插入人類基因提高了異種器官與人體免疫相容性,并降低了動物内源性病毒的傳染風險。
基因技術破解部分阻礙
即使面臨的問題還有很多,但在基因編輯技術的加持下,異種器官移植似乎為患者們推開了一扇窗。
所有器官移植都要面臨的主要障礙,在于人類自身免疫系統“清除異己”的行為。一旦有“外來物”進入人體,免疫系統就會對“外來物”發起攻擊和排斥,幾分鐘内移植的器官就可能被摧毀。這種超急性的排斥反應,不僅出現在異種器官移植中,在人與人之間的器官移植中也難以避免。
為應對超急性排斥反應,科學家曾試圖通過清除供體的抗原,或利用血液透析去掉受體體内的抗體等方式進行動物實驗,但這些方法收效甚微。随着基因技術的發展,尤其是基因編輯技術CRISPR/Cas9 的出現,科學家可以“敲除”某種基因實作更比對的器官移植供體。
同時,研究人員也向豬體内添加人類基因,讓豬器官移植到人體内後,可産生正常運作的蛋白質,如能抑制血液凝固的人血栓調節蛋白,能使器官免受宿主抗體免疫應答攻擊的 CD46。
異種器官移植潛在的病毒傳播風險是相當棘手的。目前研究确定有 26 種存在種間交叉感染風險的病原體,其中包括豬内源性逆轉錄病毒(PERV)。雖然目前沒有關于 PERV 在人體内緻病的相關報道,但 PERV 仍是全球監管機構主要擔憂的問題之一。
不能因異體器官移植“搞出”新的病毒傳播。為打消憂慮,科學家再次使用基因“敲除”的方法,實作了一次性敲除隐藏在基因組中的 PERV 片段,病毒感染率降到原來的千分之一。
▲一頭豬的器官可廣泛用于人體角膜、皮膚、胰島、關節、肌腱、韌帶、腎髒、心髒、肝髒等器官的移植(圖檔來源:Nature)
2017 年,哈佛大學教授喬治·丘奇和楊璐菡團隊在《科學》雜志發表了研究成果。他們培育出了世界上首批不帶内源性逆轉錄病毒的豬,從根本上解決了豬器官移植至人體可能導緻病毒傳染的風險。第二年,進一步解決異種器官移植免疫排斥問題的 2.0版轉基因豬誕生。此後,結合前兩代優勢的 3.0 版轉基因豬,在異種器官移植的安全性和有效性上更進一步。
▲楊璐菡團隊進行基因編輯改造的“豬3.0”(圖檔來源:Nature)
通過已知的豬和人的免疫系統關鍵的基因位點,科學家都能利用基因編輯來解決。開篇提到的全球首例豬心髒移植到人體手術中用到的豬心髒,就經過了 10 個基因修改,包括敲除 1 個控制器官生長的基因,3 個人類免疫排斥的基因,同時插入了 6 個使豬心髒可以更好地适應人體免疫系統的基因。
當然,為了得到這樣的理想中的器官移植供體,它們的生活環境有必要保持完全無菌、無病毒的“隔絕”狀态。可以想象,在一個超潔淨的豬舍内,身上配有電子晶片的它們,被 24 小時地監控,吃着經過無菌無毒處理的飼料和水,按時接受檢疫檢驗……所有這一切必然需要大量的财力、物力投入。
繞不開的倫理挑戰
當然,從解決器官移植“供不應求”沖突的角度出發,技術和金錢的難題應該都是可解的。那麼關于倫理的争議又該如何面對呢?
移植豬器官的人類算不算是“混合體”?關于這一問題,南京醫科大學的戴一凡教授曾以個人角度回應,他認為,“就像汽車換了發動機,還是原來那個牌子的汽車,本質沒發生變化。如果說人換上豬心髒就成了豬人,那麼體内裝上人工裝置的患者就成機器人了嗎?”動物器官的記憶會不會移植給人?臨床實驗中,移植年輕人腎髒的長者,頭發會變黑,移植脾氣暴躁者的心髒,溫和的人脾氣變得暴躁……如果器官真的有“記憶”,那麼異種器官會對人的生理和心理産生怎樣的影響?
▲像生産肉腸那樣“生産”器官以供給人類進行移植!這并非是天方夜譚,那些科幻片中的情節正在成為現實(圖檔來源:Nature)
此外,不同動物壽命也不一樣。一般豬的壽命在 15 年左右,那麼移植豬器官是不是會加速受體的老化呢?關于異種器官移植的基因編輯的最大限度在哪裡?動物器官具備了一定比例的人類細胞,那該稱呼“它”還是“他”?
(文章來源:綜合自知識分子知乎專欄、科學公會知乎專欄、新華網)
出品:科普中央廚房
監制:北京科技報 | 北科傳媒
歡迎分享到朋友圈
未經授權謝絕轉載